La FDA aprueba un nuevo antibacteriano
La Administración de Medicamentos y Alimentos de los Estados Unidos (FDA) aprobó hoy Fetroja (cefiderocol), un medicamento antibacteriano para el tratamiento de pacientes de 18 años de edad o mayores con infecciones complicadas del tracto urinario (cUTI), incluidas infecciones renales causadas por microorganismos gram-negativos susceptibles, que tienen enfermedades limitadas o que no tienen opciones de tratamiento alternativas.
John Farley, M.D., M.P.H., director interino de la Oficina de Enfermedades Infecciosas en el Centro de Evaluación e Investigación de Medicamentos de la FDA advirtió que “un desafío global clave al que se enfrenta la FDA como agencia de salud pública es abordar la amenaza de infecciones resistentes a los antimicrobianos, como las cUTI. Esta aprobación representa otro paso adelante en los esfuerzos generales de la FDA para garantizar que los medicamentos antimicrobianos seguros y efectivos estén disponibles para los pacientes para el tratamiento de infecciones “.
La seguridad y efectividad de Fetroja se demostró en un estudio de 448 pacientes con cUTI. De los pacientes que recibieron Fetroja, el 72,6% resolvió los síntomas y la erradicación de la bacteria aproximadamente siete días después de completar el tratamiento, en comparación con el 54,6% de los pacientes que recibieron un antibiótico alternativo. Las tasas de respuesta clínica fueron similares entre los dos grupos de tratamiento.
El etiquetado de Fetroja incluye una advertencia sobre la tasa de mortalidad por todas las causas más alta observada en pacientes tratados con Fetroja en comparación con los tratados con otros antibióticos en un ensayo en pacientes críticos con infecciones bacterianas gramnegativas resistentes a múltiples fármacos. La causa del aumento de la mortalidad no se ha establecido. Algunas de las muertes fueron el resultado del empeoramiento o las complicaciones de la infección, o las comorbilidades subyacentes. La mayor tasa de mortalidad por todas las causas se observó en pacientes tratados por neumonía adquirida en el hospital, infecciones del torrente sanguíneo o sepsis. La seguridad y eficacia de Fetroja no se ha establecido para el tratamiento de este tipo de infecciones.
Las reacciones adversas más comunes observadas en pacientes tratados con Fetroja incluyeron diarrea, estreñimiento, náuseas, vómitos, elevaciones en las pruebas hepáticas, erupción cutánea, reacciones en el lugar de infusión, candidiasis (infección por hongos), tos, dolor de cabeza e hipocalemia (bajo contenido de potasio). Fetroja no debe usarse en personas con antecedentes conocidos de hipersensibilidad grave a los fármacos antibacterianos betalactámicos.
Fetroja recibió la designación de producto calificado de enfermedades infecciosas (QIDP) de la FDA. La designación QIDP se otorga a los medicamentos antibacterianos y antimicóticos destinados a tratar infecciones graves o potencialmente mortales de la Ley de seguridad e innovación de la FDA. Como parte de la designación QIDP, a Fetroja se le otorgó una Revisión prioritaria bajo la cual el objetivo de la FDA es tomar medidas sobre una solicitud dentro de un plazo acelerado.
La FDA otorgó la aprobación de Fetroja a Shionogi & Co., Ltd
Fuente: FDA
DIU, el SIU y el implante subdérmico en el Programa Médico Obligatorio
Desde ahora, las obra sociales y prepagas deberán cubrir de manera obligatoria los métodos anticonceptivos de larga duración: la colocación y extracción del dispositivo intrauterino (DIU), del sistema intrauterino de liberación de levonorgestrel (SIU) y del implante subdérmico.
“Todos estos métodos están disponibles en el sistema de salud público”, explicó la médica Silvia Oizerovich, directora de Salud Sexual y Reproductiva de la Nación. Pero ahora, la resolución publicada este jueves en el Boletín Oficial “obliga al sistema de salud privado, ya que algunas obras sociales cobraban la colocación y extracción del DIU, e incorpora los otros dos métodos”, explicó la funcionaria.
De acuerdo a las cifras oficiales, el sistema público entregó desde enero de 2018 hasta octubre de este año, 141.762 DIUs, 5.000 SIUs y 225.150 implantes subdérmicos.
En la resolución, el sistema intrauterino de liberación de levonorgestrel, conocido por sus siglas SIU se incluyó “con recomendación específicas”, aclaró Oizerovich. Esto porque su uso “es para personas con menorragia, endometriosis, adenomiosis, leiomiomas uterinos u otra enfermedad sistémica que contraindica el uso de anticonceptivos hormonales y DIU con cobre, como método anticonceptivo”.
El SIU “es un dispositivo pequeño de plástico que tiene forma de T que se coloca en el útero e impide que los espermatozoides puedan fecundar al óvulo”, explica en su web la organización no gubernamental FUSA especializada en salud sexual y reproductiva. “A diferencia del DIU, libera una muy pequeña dosis de una hormona llamada levonorgestrel que hace que el moco del cuello uterino se vuelva más espeso, impidiendo el ingreso de los espermatozoides”, añade la información.
“Con esta decisión completamos la canasta de insumos de métodos anticonceptivos gratuitos en el Programa Médico Obligatorio (PMO)”, destacó Oizerovich.
Asimismo, la funcionaria afirmó que “están garantizados los métodos en el sistema público, los estamos entregando. Puede haber algún retraso en el caso del SIU, ya que tenemos que llamar a una nueva licitación para comprarlo”.
La directora de Salud Sexual y Reproductiva señaló que “la evidencia médica a nivel internacional demostró la importancia de estos métodos anticonceptivos de larga duración que ahora incorporamos al Plan Médico Obligatorio (PMO)”. Añadió que “como informamos hace unas semanas, descendió el embarazo en chicas de 15 a 19 años, y creemos que se relaciona, primero con las consejerías en salud sexual y reproductiva, y con el uso de métodos de larga duración”.
Fuente: Página 12 / COFA
Se amplía el uso de la inmunoterapia para diferentes tipos de cáncer de pulmón
En el marco del XXIV Congreso Argentino e Internacional de Oncología Clínica llevado a cabo del 6 al 8 de noviembre en la ciudad de Rosario, se presentó la aprobación en el país de la inmunoterapia atezolizumab para el tratamiento del cáncer de pulmón de células no pequeñas no escamosas y del cáncer de pulmón de células pequeñas. Esta última patología no contaba con novedades para su tratamiento desde hacía más de 20 años.
El cáncer de pulmón se divide principalmente en dos tipos que se diferencian entre sí por el tamaño de las células bajo el microscopio: el Cáncer de Pulmón de Células No Pequeñas (CPCNP), que afecta al 85% de los pacientes diagnosticados con la enfermedad, y el Cáncer de Pulmón de Células Pequeñas (CPCP), que se presenta en el 15% de los casos.
En la actualidad, la inmunoterapia se ha convertido en la innovación más reciente y significativa para el tratamiento oncológico y para diferentes tipos de cáncer de pulmón. Su función es ayudar al sistema inmune a reconocer las células cancerosas para poder atacarlas ya que en muchos casos estas mismas células logran evadir la respuesta inmunitaria natural del organismo y desarrollarse hasta convertirse en tumores potencialmente peligrosos.
La aprobación de atezolizumab combinado con quimioterapia (basada en carboplatino y etopósido) como primera línea de tratamiento para cáncer de pulmón de células pequeñas, se basa en los resultados del estudio de fase III “IMpower 133”, donde se demostró que esta combinación mejora la supervivencia global, en los pacientes con esta patología en estado avanzado, en comparación con el tratamiento basado únicamente en quimioterapia.
Esta nueva opción terapéutica no solo prolonga la expectativa de vida sino que les brinda a los pacientes una mejor calidad de vida.
“Hace más de 20 años que no teníamos novedades en este tipo de cáncer de pulmón, solo dependíamos de que el paciente respondiera al tratamiento de quimioterapia convencional. Muchas drogas en investigación fallaron, por esto creemos desde la oncología que ésta es una muy buena noticia. Esta nueva combinación demostró una supervivencia global con excelente calidad de vida y tolerancia al tratamiento ya que no genera mayores efectos colaterales”, expresó el Prof. Dr. Diego Lucas Kaen (M.P. 1898), Director de Investigación Clínica del Centro Oncológico Riojano Integral y Docente de la Universidad Nacional de La Rioja.
El adenocarcinoma es el subtipo más frecuente del cáncer de pulmón de células no pequeñas (CPCNP), y representa el 40% de los casos. La aprobación de la inmunoterapia atezolizumab, en combinación con bevacizumab y cuatro ciclos de quimioterapia (carboplatino y paclitaxel), se basa en los resultados del estudio de fase III denominado “IMpower 150”.Los mismos demostraron un beneficio de supervivencia significativo en comparación al mismo tratamiento sin la inmunoterapia. El estudio observó un beneficio en la supervivencia global y una disminución del riesgo de progresión y muerte en todos los pacientes con esta patología, ya sea que expresen o no la proteína PD-L1 (causante de que el sistema inmune no actúe sobre las células tumorales) y en poblaciones clave como pacientes con metástasis hepáticas.
Los desafíos en el tratamiento del cáncer de pulmón continúan siendo un importante motivo de investigación clínica. Incansablemente se estudian nuevas terapias que les permitan a los pacientes tener una mayor expectativa y calidad de vida.
“La inmunoterapia llegó para quedarse, los resultados mejoran día a día y el impacto que hay en la sobrevida global en oncología es increíble. Además, su toxicidad es diferente, claramente los pacientes la toleran mucho mejor que a la quimioterapia.Creo que tenemos muchas respuestas pero tenemos que seguir buscando otras, por eso hay que seguir investigando. Argentina es líder en la región en investigación clínica, hemos participado en todos estos estudios y lo seguiremos haciendo”, concluye Kaen.
Concepción del Uruguay: prohíben la venta de medicamentos fuera de las farmacias
El Concejo Deliberante de la ciudad de Concepción del Uruguay, Entre Ríos, promulgó la Ordenanza municipal que adhiere a la Ley Provincial 9817 que establece el expendio de medicamento solo en farmacias.
Ricardo Gargano, presidente del Círculo de Farmacéuticos de Concepción del Uruguay, (ER) contó cómo fue el proceso para lograr concientizar a los representantes sobre la importancia sanitaria de la medida. “Fueron varios meses de trabajo. Inicialmente concertamos una entrevista con el Secretario de Salud municipal, Dr. Sergio Bertolotti, presentamos en el Honorable Concejo Deliberante (HCD) el pedido de audiencia, y en reuniones siguientes ampliamos nuestra presentación, defendiendo la propuesta. En la evolución de este proyecto conocimos a varios miembros del Consejo, entre ellos al Dr. Hugo Cettour, ex ministro de Salud, y al Dr. Martín Oliva, intendente electo de Concepción del Uruguay”.
El dirigente entrerriano expresó: “Lo logrado fue el fruto de un trabajo en equipo. Quiero resaltar el apoyo de mis colegas en general, entre los que se destacan Itati Moren con su acompañamiento incondicional, y Alberto Villalba quien nos orientó con su vasta experiencia en este tema, compartiendo cada reunión junto a nosotros. Nuestro próximo paso es la difusión masiva del concepto del medicamento solo dispensado en farmacias, para lograr una sociedad más sana y protegida por los custodios del medicamento: los farmacéuticos”.
Fuente: COFA
Por primera vez Argentina preside la Federación Farmacéutica Sudamericana
En el marco del XXI Congreso de la Federación Farmacéutica Sudamericana (FEFAS) que se está desarrollando en Ciudad del Este, Paraguay, fue electa la Farm. Marcela Ruiz, presidente del Colegio de Farmacéuticos de Salta, en el cargo de presidente de la Federación Farmacéutica Sudamericana. Están presentes en la Asamblea la presidente de la COFA, María Isabel Reinoso y la secretaria, Alicia Merlo, quienes presentaron la postulación de la Farm. Ruiz para presidir la federacion regional.
La FDA aprueba el primer tratamiento para H. pylori a base de rifabutina
La Administración de Medicamentos y Alimentos de los Estados Unidos (FDA) aprobó Talicia (RedHill Biopharma Ltd), el primer tratamiento a base de rifabutina para la infección por Helicobacter pylori (H pylori) en adultos.
Cada cápsula de liberación retardada de Talicia contiene omeprazol 10mg (equivalente a 10.3mg de omeprazol magnesio), amoxicilina 250mg y rifabutina 12.5mg.
“Los estudios con Talicia encontraron resistencia cero a la rifabutina y mostraron una resistencia del 17% a la claritromicina, un antibiótico macrólido estándar de atención actual, consistente con los datos actuales que muestran que las terapias que contienen claritromicina fallan en aproximadamente del 25% al 40% de los casos “, dijo David Graham, investigador del Baylor College of Medicine en Texas, quien lideró los estudios en fase 3.
Los dos estudios de fase 3 incluyeron adultos con H pylori positivo que se quejaban de dolor y / o molestias epigástricas.
En el ensayo confirmatorio de fase 3, 4 de 305 pacientes (1%) tratados con Talicia interrumpieron la medicación debido a una reacción adversa, informó la compañía. Las reacciones adversas que condujeron a la interrupción fueron náuseas y vómitos, congestión nasal y nasofaringitis.
La compañía proyecta lanzar Talicia en los Estados Unidos en el primer trimestre de 2020.
Fuente: Medscape / COFA
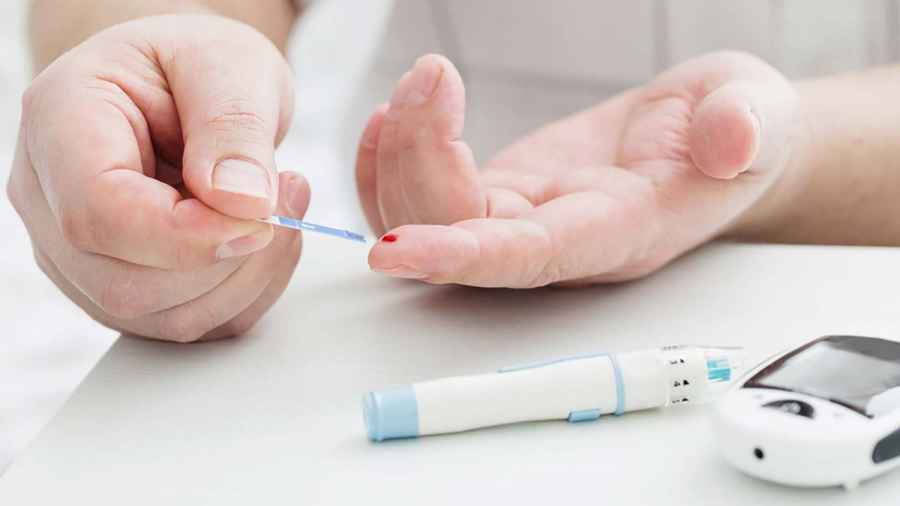
Diabetes: 1 de cada 2 personas no está diagnosticada
La Sociedad Argentina de Diabetes (SAD) lanza una campaña de difusión y concientización a nivel nacional sobre esta enfermedad, que a nivel global afecta a más de 425 millones de adultos. Con ella, se busca que quienes la tengan gocen de una mejor calidad de vida con la menor cantidad de limitaciones posibles, y quienes presenten síntomas, o los factores de riesgo para desarrollar la forma más común de la enfermedad (la diabetes tipo 2), realicen las consultas correspondientes. Dicha activación también implicará la iluminación de color azul de monumentos y lugares históricos de diferentes lugares del país el próximo 14 de noviembre.
Según el último estudio realizado en 2017 de la Federación Internacional de la Diabetes, para el año 2045 el número de afectados ascenderá a 629 millones. En Argentina, la prevalencia de diabetes es del 11% (+4M de personas), y continúa creciendo: según la Cuarta Encuesta Nacional de Factores de Riesgos, realizada en 2019 por la Dirección Nacional de Promoción de la Salud y Control de Enfermedades Crónicas No Transmisibles, hubo un incremento de casi 3 puntos respecto a la última medición realizada en 2013. Asimismo, se registró un aumento en los porcentajes de otros factores de riesgo asociados a la enfermedad como obesidad (20,8 a 25,4), el exceso de peso (sobrepeso + obesidad; 57,9 a 61,6), baja actividad física (54,7 a 64,9) y presión arterial elevada (34,1 a 34,6).
Las estadísticas indican que la proporción de personas con diabetes tipo 2 se incrementa en casi todos los países y coinciden en que 1 de cada 2 de quienes padecen diabetes no están diagnosticadas.
En línea con ello, menos del 50% de las personas con la enfermedad tienen un buen control glucémico.
Partiendo de la base de que la diabetes tipo 2 es prevenible, los profesionales de la salud aseguran que implementando buenos hábitos como una alimentación balanceada, con las porciones adecuadas, y la realización de actividad física, se reducen los factores de riesgo como el sedentarismo, el sobrepeso, la obesidad y la presión arterial elevada.
Si no se trata, la diabetes puede afectar, entre otras cosas, la visión, la presión arterial, el corazón, los riñones y todo el sistema nervioso. Además de la alimentación, la actividad física y el tratamiento farmacológico, es fundamental promover la educación diabetológica del paciente y su entorno para una óptima calidad de vida. Sin embargo, una de las mayores preocupaciones que tienen hoy en día los profesionales es la adherencia de las personas con diabetes al tratamiento, que muchos aseguran, no sostienen en el tiempo.
#ActuarHoyAnteLaDiabetes es una campaña a nivel global de Servier, laboratorio que acompaña la acción local para concientizar y educar a la comunidad sobre esta enfermedad, cuyos pilares son destacar la importancia de la prevención, el diagnóstico y el tratamiento para evitar complicaciones de riesgo.
El sarampión elimina la memoria inmune del organismo hasta tres años
Durante la última década se ha acumulado evidencia de que la vacuna contra el sarampión protege de dos maneras ya que, no solo previene la enfermedad aguda que con frecuencia envía a los niños al hospital, sino que también parece proteger contra otras infecciones a largo plazo. Los investigadores han descubierto ahora el mecanismo y el alcance de la amnesia inmune inducida por el sarampión a raíz de la infección.
Algunos investigadores han sugerido que la vacuna da un impulso general al sistema inmune. Otros plantearon la hipótesis de que los efectos protectores extendidos de la vacuna provienen de la prevención de la infección por sarampión.
Según esta teoría, el virus puede dañar la memoria inmune del cuerpo, causando la llamada amnesia inmune. Al proteger contra la infección de sarampión, la vacuna evita que el cuerpo pierda u “olvide” su memoria inmune y preserva su resistencia a otras infecciones.
Investigaciones anteriores insinuaron los efectos de la amnesia inmune, mostrando que la supresión inmune después de la infección por sarampión podría durar hasta dos o tres años. Sin embargo, muchos científicos aún debaten qué hipótesis es correcta ya que, si la amnesia inmune es real, cómo sucede exactamente y cómo es de grave.
Ahora, un estudio de un equipo internacional de investigadores dirigido por investigadores de la Escuela de Medicina de Harvard, el Hospital Brigham and Women’s y la Escuela de Salud Pública de Harvard TH Chan, publicado en la revista ‘Science’, proporciona respuestas.
Los investigadores muestran que el virus del sarampión elimina del 11 al 73 por ciento de los diferentes anticuerpos que protegen contra las cepas virales y bacterianas a las que una persona era previamente inmune, desde la gripe hasta virus del herpes o bacterias que causan neumonía e infecciones de la piel.
Entonces, si una persona tenía 100 anticuerpos diferentes contra la varicela antes de contraer sarampión, podría salir de tener sarampión con solo 50, reduciendo a la mitad su protección contra la varicela. Esa protección podría disminuir aún más si algunos de los anticuerpos perdidos son defensas potentes conocidas como anticuerpos neutralizantes.
El estudio es el primero en medir el daño inmune causado por el virus y subraya el valor de prevenir la infección por sarampión mediante la vacunación
“La amenaza que representa el sarampión para las personas es mucho mayor de lo que imaginamos anteriormente –apunta el autor principal Stephen Elledge, profesor de Genética y Medicina Gregor Mendel en el Instituto Blavatnik de la Facultad de Medicina de Harvard y el Hospital Brigham and Women’s–. Ahora entendemos que el mecanismo es un peligro prolongado debido a la eliminación de la memoria inmune, lo que demuestra que la vacuna contra el sarampión es aún más beneficiosa de lo que sabíamos”.
El descubrimiento de que el sarampión agota los repertorios de anticuerpos de las personas, destruyendo parcialmente la memoria inmune a la mayoría de los patógenos encontrados anteriormente, respalda la hipótesis de la amnesia inmune.
“Esta es la mejor evidencia hasta ahora de que existe amnesia inmune e impacta nuestra memoria inmune de buena fe a largo plazo”, agrega Mina, quien descubrió por primera vez los efectos epidemiológicos del sarampión en la mortalidad infantil a largo plazo en un artículo de 2015.
El trabajo del equipo fue publicado simultáneamente con un artículo de un equipo separado en ‘Science Immunology’ que llegó a conclusiones complementarias al medir los cambios en las células B causados por el virus del sarampión. Un editorial acompañante en ‘Science Immunology’, escrito por Duane Wesemann, profesor asistente de medicina de la Facultad de Medicina de Harvard en el Hospital Brigham and Women’s, contextualiza ese estudio.
Elledge, Mina y sus colegas descubrieron que aquellos que sobreviven al sarampión recuperan gradualmente su inmunidad previa a otros virus y bacterias a medida que se vuelven a exponer a ellos. Pero debido a que este proceso puede llevar meses o años, las personas siguen siendo vulnerables mientras tanto a las complicaciones graves de esas infecciones.
A la luz de este hallazgo, los investigadores dicen que los médicos pueden considerar fortalecer la inmunidad de los pacientes que se recuperan de la infección por sarampión con una ronda de inyecciones de refuerzo de todas las vacunas de rutina anteriores, como la hepatitis y la poliomielitis.
“La revacunación después del sarampión podría ayudar a mitigar el sufrimiento a largo plazo que podría derivarse de la amnesia inmune y la mayor susceptibilidad a otras infecciones”
Según la Organización Mundial de la Salud, el sarampión, una de las enfermedades más contagiosas conocidas por la humanidad, mató a 2,6 millones de personas de media cada año antes de que se desarrollara una vacuna.
La vacunación generalizada ha reducido el número de muertes pero la falta de acceso a la vacuna y la negativa a vacunarse significa que el sarampión todavía infecta a más de 7 millones de personas y mata a más de 100.000 cada año en todo el mundo, informa la OMS, y los casos están en aumento, triplicándose a principios de 2019.
Investigaciones epidemiológicas previas sobre la amnesia inmune sugieren que las tasas de mortalidad atribuidas al sarampión podrían ser aún mayores, representando hasta el 50 por ciento de toda la mortalidad infantil, si los investigadores tuvieran en cuenta las muertes causadas por infecciones causadas por los efectos devastadores del sarampión en la inmunidad.
Este nuevo descubrimiento fue posible gracias a ‘VirScan’, una herramienta de Elledge y Tomasz Kula, estudiante de doctorado en Elledge Lab, desarrollado en 2015. Detecta anticuerpos antivirales y antibacterianos en la sangre que resultan de encuentros actuales o pasados con virus y bacterias, dando una imagen general del sistema inmune.
Los autores destacan que los efectos observados en el estudio actual ocurrieron en niños previamente sanos. Debido a que se sabe que el sarampión afecta mucho más a los niños desnutridos, el grado de amnesia inmune y sus efectos podrían ser aún más graves en poblaciones menos saludables.
“El niño promedio podría salir del sarampión con una ‘abolladura’ en su sistema inmunológico y su cuerpo podrá manejar eso –ejemplifica Elledge–. Pero los niños al límite, como aquellos con infección grave de sarampión o deficiencias inmunes o aquellos que están desnutridos, tendrán serios problemas”.
Los resultados se alinean con décadas de investigación. Asegurar la vacunación generalizada contra el sarampión no solo ayudaría a prevenir las 120.000 muertes que se atribuirán directamente al sarampión solo este año, sino que también podría evitar potencialmente cientos de miles de muertes adicionales atribuibles al daño duradero del sistema inmune, recuerdan los autores.
“Esto destaca la importancia de comprender y prevenir los efectos a largo plazo del sarampión, incluidos los efectos silenciosos que han pasado desapercibidos para los médicos y los padres –advierte Mina–. Si su hijo contrae el sarampión y luego contrae neumonía dos años después, no necesariamente los uniría, pero los síntomas del sarampión en sí pueden ser solo la punta del iceberg”.
Fuente: Europa Press / COFA
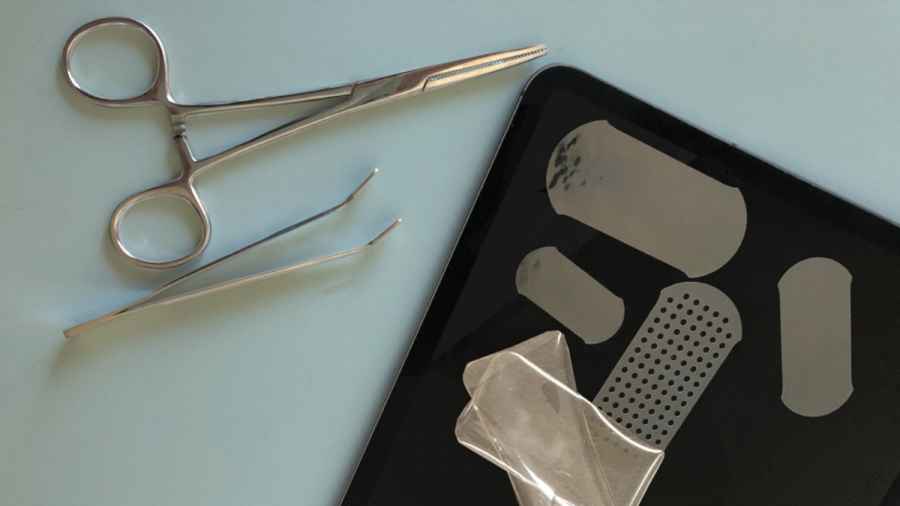
Diseñan una cinta de doble cara para tejidos que podría reemplazar las suturas
Inspirados en una sustancia pegajosa que las arañas usan para atrapar a sus presas, ingenieros del Instituto Tecnológico de Massachusetts (MIT) diseñaron una ‘cinta de doble cara’ que puede sellar rápidamente los tejidos en cuestión de segundos y podría sustituir en un futuro las suturas quirúrgicas, según publican en la revista ‘Nature’.
En pruebas en ratas y tejidos de cerdo, los investigadores demostraron que su nueva cinta puede unirse firmemente a tejidos como los pulmones y los intestinos en solo cinco segundos. Esperan que esta cinta pueda usarse en lugar de las suturas, que no funcionan bien en todos los tejidos y pueden causar complicaciones en algunos pacientes.
“Hay más de 230 millones de cirugías importantes en todo el mundo por año, y muchas de ellas requieren suturas para cerrar la herida, lo que en realidad puede causar estrés en los tejidos y puede causar infecciones, dolor y cicatrices. Estamos proponiendo un enfoque fundamentalmente diferente para sellar tejidos”, explica Xuanhe Zhao, autor principal del estudio.
Los investigadores mostraron que la cinta de doble cara también se puede usar para unir dispositivos médicos implantables a los tejidos, incluido el corazón.
Además, funciona mucho más rápido que los pegamentos de tejido, que generalmente tardan varios minutos en unirse firmemente y pueden gotear sobre otras partes del cuerpo.
Se considera muy difícil formar un sello hermético entre los tejidos porque el agua en la superficie de los tejidos interfiere con la adhesión. Los pegamentos de tejido existentes difunden moléculas adhesivas a través del agua entre dos superficies de tejido para unirlas, pero este proceso puede llevar varios minutos o incluso más.
El equipo del MIT quería idear algo que funcionara mucho más rápido. El grupo de Zhao había desarrollado previamente otros adhesivos novedosos, incluido un superpegamento de hidrogel que proporciona una adhesión más dura que los materiales pegajosos que se producen en la naturaleza, como los que usan los mejillones y los percebes para adherirse a barcos y rocas.
Para crear una cinta de doble cara que pudiera unir rápidamente dos superficies húmedas, el equipo se inspiró en el mundo natural, específicamente, el material adhesivo que las arañas usan para capturar a sus presas en condiciones húmedas. Este pegamento de araña incluye polisacáridos cargados que pueden absorber agua de la superficie de un insecto casi instantáneamente, creando un pequeño parche seco al que se puede adherir el pegamento.
Para imitar esto, los investigadores diseñaron un material que primero absorbe agua de los tejidos húmedos y luego une rápidamente dos tejidos. Para la absorción de agua, usaron ácido poliacrílico, un material muy absorbente que se usa en pañales. Tan pronto como se aplica la cinta, absorbe agua, permitiendo que el ácido poliacrílico forme rápidamente enlaces de hidrógeno débiles con ambos tejidos.
Estos enlaces de hidrógeno y otras interacciones débiles mantienen temporalmente la cinta y los tejidos en su lugar, mientras que los grupos químicos llamados ésteres del NHS, que los investigadores incorporaron en el ácido poliacrílico, forman enlaces mucho más fuertes, llamados enlaces covalentes, con proteínas en el tejido. Esto lleva unos cinco segundos.
Para hacer que su cinta sea lo suficientemente resistente como para durar dentro del cuerpo, los investigadores incorporaron gelatina o quitosano (un polisacárido duro que se encuentra en los caparazones de los insectos). Estos polímeros permiten que el adhesivo mantenga su forma durante largos períodos de tiempo.
Dependiendo de la aplicación para la que se usa la cinta, los investigadores pueden controlar qué tan rápido se descompone dentro del cuerpo variando los ingredientes que entran. La gelatina tiende a descomponerse en unos pocos días o semanas en el cuerpo humano, mientras que el quitosano puede durar más (un mes o incluso hasta un año).
Este tipo de adhesivo podría tener un gran impacto en la capacidad de los cirujanos para sellar incisiones y curar heridas, dice el estudiante de posgrado Hyunwoo Yuk. Para explorar posibles aplicaciones para la nueva cinta de doble cara, los investigadores la probaron en algunos tipos diferentes de tejido de cerdo, incluida la piel, el intestino delgado, el estómago y el hígado.
También realizaron pruebas en pulmones de cerdo y tráquea, demostrando que podían reparar rápidamente el daño a esos órganos. “Es muy difícil suturar tejidos blandos o frágiles como el pulmón y la tráquea, pero con nuestra cinta adhesiva de doble cara, en cinco segundos podemos sellarlos fácilmente”, añade Yuk.
La cinta también funcionó bien para sellar el daño al tracto gastrointestinal, lo que podría ser muy útil para prevenir fugas que a veces ocurren después de la cirugía que pueden causar sepsis y otras complicaciones potencialmente fatales.
Implantar dispositivos médicos dentro del cuerpo es otra aplicación que el equipo del MIT está explorando, como un parche cardíaco de poliuretano. Normalmente, este tipo de procedimiento es extremadamente complicado y requiere la realización de un cirujano experimentado, pero el equipo de investigación, en ensayo en ratas, pudo simplemente pegar el parche con su cinta presionando durante unos segundos y permaneció en su lugar durante varios días. Además, los investigadores descubrieron que la cinta podía unir con éxito materiales como caucho de silicona, titanio e hidrogeles a los tejidos.
“Esto proporciona una forma más directa y más universalmente aplicable de introducir un monitor implantable o un dispositivo de administración de medicamentos, porque podemos adherirnos a muchos sitios diferentes sin causar daños o complicaciones secundarias por la perforación del tejido para fijar los dispositivos”, señala Yuk.
Los investigadores ahora están trabajando con médicos para identificar aplicaciones adicionales para este tipo de adhesivo y realizar más pruebas en modelos animales.
Fuente: Europa Press / COFA
La Comisión Europea aprueba XOSPATA
La Comisión Europea (CE) ha aprobado el medicamento XOSPATA (gilteritinib) de Astellas como monoterapia para el tratamiento de pacientes adultos con leucemia mielógena aguda (LMA) refractaria o recidiva con mutaciones del FLT3 (FLT3 mut+) detectadas usando el ensayo de mutación LeukoStrat CDx FLT3 de Invivoscribe.
La prueba de LeukoStrat está disponible como servicio de línea de prueba a través de las subsidiarias de Invivoscribe, LabPMM LLC (San Diego, California, EE. UU.), LabPMM GmbH (Martinsried, Alemania) y LabPMM GK (ciudad de Kawasaki, Japón). Los kits de los ensayos de mutación LeukoStrat CDx FLT3 también se están distribuyendo actualmente en Europa, Japón, Suiza y Australia, con planes futuros de distribución en Estados Unidos y China.
Invivoscribe desarrolló el ensayo de mutación LeukoStrat CDx FLT3 en conjunto con Astellas como diagnóstico complementario para predecir las respuestas de los pacientes al medicamento de Astellas Pharma para LMA, XOSPATA (fumarato de gilteritinib).
Esta aprobación se basa en los resultados del ensayo ADMIRAL Fase 3 que investigó gilteritinib comparado con quimioterapia de rescate en pacientes con LMA refractaria o recidiva con mutación FLT3.
Los pacientes tratados con gilteritinib tuvieron supervivencia general (SG) significativamente mayor que los que recibieron quimioterapia de rescate. La SG media para pacientes que recibieron gilteritinib fue de 9,3 meses, comparada con 5,6 meses para pacientes que recibieron solamente quimioterapia de rescate.
Este hito consolida más aún al ensayo de mutación LeukoStrat CDx FLT3 como el estándar internacional para evaluación integral del FLT3 para pacientes gravemente enfermos de LMA dado que este diagnóstico complementario (CDx) identifica las mutaciones ITD y TKD FLT3 y está disponible en todo el mundo.
Esta aprobación complementa previas aprobaciones regulatorias de Invivoscribe del ensayo de mutación LeukoStrat CDx FLT3 como diagnóstico complementario para XOSPATA (fumarato de gilteritinib) para Astellas, RYDAPT (midostaurina) para Novartis y clorhidrato de quizartinib para Daiichi Sankyo.
"La aprobación de la Comisión Europea marca un importante avance para pacientes con leucemia mielógena aguda recidiva o refractaria con mutación positiva del FLT3. Invivoscribe ve con alegría más opciones de tratamiento disponibles para prolongar la vida de los pacientes, celebra las asociaciones con compañías farmacéuticas interesadas en aprovechar nuestro programa Streamlined CDx, para acelerar las aprobaciones de medicamentos en todo el mundo, sea que sus terapias estén dirigidas a enfermedades hematológicas o a tumores sólidos", dijo Jeffrey Miller, CEO y director general de Ciencias de Invivoscribe.
Acerca del ensayo de mutación LeukoStrat CDx FLT3 de Invivoscribe
El ensayo de mutación LeukoStrat CDx FLT3 es una prueba diagnóstica in vitro basada en PCR diseñada para detectar mutaciones internas de duplicación en tándem (ITD) y mutaciones del dominio de la tirosina quinasa (TKD) D835 e I836 en el gen FLT3 del ADN genómico extraído de células mononucleares obtenidas a partir de sangre periférica o de aspirados de médula ósea de pacientes diagnosticados con leucemia mielógena aguda.
El ensayo de mutación LeukoStrat CDx FLT3 se utiliza como ayuda en la evaluación de pacientes con LMA para los que se está considerando el tratamiento con Midostaurin (Estados Unidos, Europa, Suiza y Australia).
El ensayo de mutación LeukoStrat CDx FLT3 se utiliza como ayuda en la evaluación de pacientes con LMA para los que se está considerando el tratamiento con fumarato de gilteritinib (Estados Unidos, Europa y Japón).
El ensayo de mutación LeukoStrat CDx FLT3 se utiliza como ayuda en la evaluación de pacientes con LMA para los que se está considerando el tratamiento con clorhidrato de quizartinib (Japón).
Esta prueba estandarizada a nivel mundial incluye un software que interpreta datos, genera relaciones de señal mutante/tipo salvaje para mutaciones ITD y TKD. Este ensayo ampliamente validado ayuda a estandarizar la detección de mutaciones genéticas en el gen FLT3 como una de las mutaciones conductoras más importantes de la leucemia mielógena aguda (LMA).
FUENTE Invivoscribe, Inc / PR Newswire
Lo más visto
- Covishield, la vacuna que India lanzó con Oxford-AstraZeneca
- El gobierno establece los requisitos para la producción de cannabis medicinal
- Anmat aprobó en el país la primera vacuna que protege contra el dengue
- Comunicación de Novo Nordisk: Diferencias en la indicación de Victoza® y Saxenda®
- Ibupirac declarado apto para celíacos